製品・安全性 よくあるご質問
- ここに掲載のQ&Aは、医療従事者向けの内容です。
- この情報は、製品の適正使用に関する参考情報であり、あらゆるケースに適応されるものではありません。
従いまして、 Q&Aの利用によって生じた結果については、責任を負いかねますのでご了承ください。なお、製品のご使用に当たっては、最新の電子添文/添付文書をご確認ください。 - 製品に関してご不明な点がございましたら、弊社お問い合わせ窓口又は弊社担当MRにお問い合わせください。
オフサグリーン
特殊背景患者
妊婦へ投与できますか?
オフサグリーン静注用は妊産婦への使用経験がなく安全性が十分検討されていません。妊婦又は妊娠している可能性のある女性には、診断上の有益性が危険性を上回ると判断される場合にのみ投与してください。
- 【参考】
- 眼底血管造影実施基準(改訂版)1)
- 妊娠中の投与に関しては安全性が確立していないので、投与は避けるべきである。検査によって得られる情報による診断上の有益性が危険性を上回ると判断される場合には、十分に説明しインフォームドコンセントを取得して検査を行うと記載されている。
- 生殖発生毒性試験2)
- 妊娠マウス、ラットの器官形成期にインドシアニングリーン5~40mg/kgを静脈内投与して、胎児の外部異常、骨格異常、新生児の産児数、発育状態、哺育率等を検討した結果、いずれも異常は認められず、インドシアニングリーンに催奇形作用は認められなかった。
- 血液‐胎盤関門通過性3)
- (外国人データ)
分娩中の妊婦(8例)にインドシアニングリーン5mg/kgを静脈内投与したとき、母体の血中濃度は投与後2~4分で2.59~4.80mg%、6~8分で1.08~3.68mg%であったが、胎児頭皮血液及び生後直ちに採取された臍静脈血液中濃度は検出限界以下(0.02mg%)であった。
- 参考資料
-
- 1)湯澤美都子:日本眼科学会雑誌 115, 67(2011)【62599】
- 2)オフサグリーン静注用25mg インタビューフォーム Ⅸ-2.-(5) 生殖発生毒性試験の項
- 3)オフサグリーン静注用25mg インタビューフォーム Ⅶ-5.-(2) 血液-胎盤関門通過性の項
[2023/11 更新]
授乳婦へ投与できますか?
オフサグリーン静注用の授乳中の女性への投与は、診断上の有益性および母乳栄養の有益性を考慮し、授乳の継続又は中止を判断してください。乳児への影響が懸念される場合には授乳を中止し、人工母乳に切り替えてください。
- 【参考】
- 眼底血管造影実施基準(改訂版)1)
- 蛍光造影剤の授乳婦への投与は避けることが望ましいと記載されている。
- 血中濃度2)
- 健康成人(13例)にインドシアニングリーン0.25mg/kgを静脈内投与したとき、血漿中濃度推移は投与後約15分までは指数関数的に減少し、その後は減少が緩徐となり、血漿中より速やかに消失する。
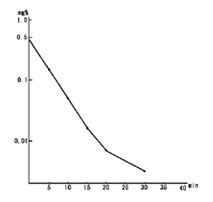
図. インドシアニングリーン血中消失曲線
(インタビューフォームより引用)
- 参考資料
-
- 1)湯澤美都子他:日本眼科学会雑誌 115, 67(2011)【62599】
- 2)オフサグリーン静注用25mg インタビューフォーム Ⅶ-1.-(2) 臨床試験で確認された血中濃度の項
[2023/11 更新]
小児等(新生児、乳児、幼児、小児)へ投与できますか?
オフサグリーン静注用は小児等を対象とした臨床試験は実施しておらず、安全性は確立していません。診断上の有益性が危険性を上回ると判断される場合にのみ投与してください。
※年齢区分(おおよその目安)
小児:7歳以上、15歳未満の児、幼児:1歳以上、7歳未満の児、乳児:生後4週以上、1歳未満の児、新生児:出生後4週未満の児、低出生体重児:出生時の体重が2500g未満の児
- 【参考】
- 眼底血管造影実施基準(改訂版)1)
- (小児等の症例に対して眼底血管造影)検査を実施する場合には検査の必要性と安全性を慎重に判断すると記載されている。
- 使用成績調査2)
- オフサグリーン静注用の使用成績調査の結果では、15歳未満の小児は1例であり、副作用の発現は認められなかった。
- 参考資料
-
- 1)湯澤美都子他:日本眼科学会雑誌 115, 67(2011)【62599】
- 2)オフサグリーン静注用25mg インタビューフォーム Ⅷ-6.-(7) 小児等の項
[2023/11 更新]
安全性
検査前にビグアナイド系糖尿病薬(ブホルミン、メトホルミン)の投与を中止する必要はありますか?
オフサグリーンで検査する前にビグアナイド系糖尿病薬の投与を中止する必要はありません。ただし、オフサグリーンの副作用には悪心・嘔吐などがあり、これらの症状がビグアナイド系糖尿病薬による乳酸アシドーシスを誘発(※)したり、マスクしたりする可能性があり、併用時もビグアナイド系糖尿病薬でみられる副作用に注意が必要です。
※ビグアナイド系糖尿病薬の電子添文には、脱水による乳酸アシドーシスを起こすことがあると記載されている。
- 【参考】
- ビグアナイド系糖尿病薬とヨード造影剤は主に腎臓から排泄されます。ヨード造影剤で腎機能の低下をきたすと、ビグアナイド系糖尿病薬の排泄が低下、血中濃度が上昇するため、乳酸アシドーシスを起こすおそれがあります。このため、両剤の併用は、併用注意に設定され、ヨード造影剤を使用する場合は、ビグアナイド系糖尿病薬の投与を一時的に中止することとなっています。
一方、オフサグリーンに含まれるヨードはヨード造影剤と比較し少なく、またオフサグリーン静注後は速やかに肝に取り込まれ、ほとんどは糞便中に排泄されます1)。
このように体内に入るヨード量は微量で腎からの排泄もほとんどありませんので、オフサグリーンはビグアナイド系糖尿病薬と併用しても問題ないと考えられます。
- 参考資料
-
- 1)オフサグリーン静注用25mg インタビューフォーム Ⅶ-7. 排泄の項
[2023/11 更新]
その他、点眼剤の全般的な服薬指導についてはこちらをご覧ください。
製品に関するお問い合わせ(医療関係者の皆様)
製品情報センター:0120-921-839
※上記フリーコールがご利用いただけない場合:06-6321-7056
受付時間:9:00~17:00(土、日、祝日を除く)
お問い合わせフォームはこちら